IOTest Myeloid Activation CD169-PE/HLA-DR-APC/CD64-PB Antibody Cocktail Analysis of Whole Blood [RUO]
L'attivazione delle cellule mieloidi è una risposta precoce all'infezione. Le cellule mieloidi del sistema immunitario innato rispondono in modo diverso quando vengono stimolate da batteri o virus1,2. Una semplice combinazione di 3 marcatori fornisce un'eccellente panoramica dell'intera risposta immunitaria innata analizzando il sangue periferico.
Resistenza agli antibiotici. L'errata identificazione della fonte e della natura dell'infezione è una delle maggiori difficoltà, che porta all'abuso di antibiotici e alla resistenza3. La rapida identificazione delle infezioni batteriche, utilizzando l'nCD64, aiuterà la ricerca di biomarcatori e lo sviluppo di nuovi antibiotici.4
Progressione della malattia virale. Ricerche recenti hanno dimostrato che i livelli di interferone sono modulati durante il corso della malattia. La risposta IFN di tipo I, che aumenta nelle infezioni virali, come il COVID e l'HIV, diventa altamente compromessa nei soggetti gravi e critici. I marcatori cellulari come i monociti CD169 sono importanti strumenti di ricerca per comprendere l'attività dell'interferone durante l'infezione virale e la progressione della malattia.5,6,7,8
Segnalazione dell'interferone. Gli interferoni di tipo I e II (IFN) sono attori centrali nella modulazione della risposta immunitaria. Recenti evidenze hanno dimostrato che queste molecole regolano le funzioni reciproche e quelle di altre cellule immunitarie dell'immunità innata e adattativa. Sono in corso ulteriori ricerche per comprendere il ruolo svolto da queste molecole nelle infezioni, nelle malattie infiammatorie e nel cancro, soprattutto come bersagli farmacologici e biomarcatori.8,9,10
Virus versus Bacterial Immune Response1, 2
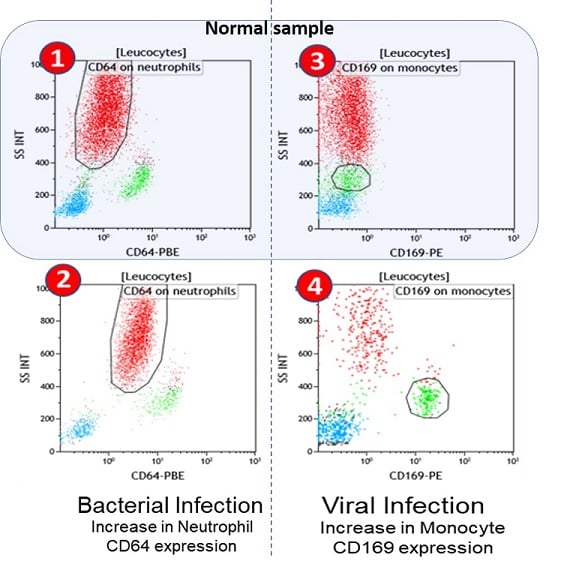
Pannelli di citofluorimentria rappresentanti l'espressione di CD64 (neutrofili) nell'infezione batterica e CD169 (monociti) nell'infezione virale.
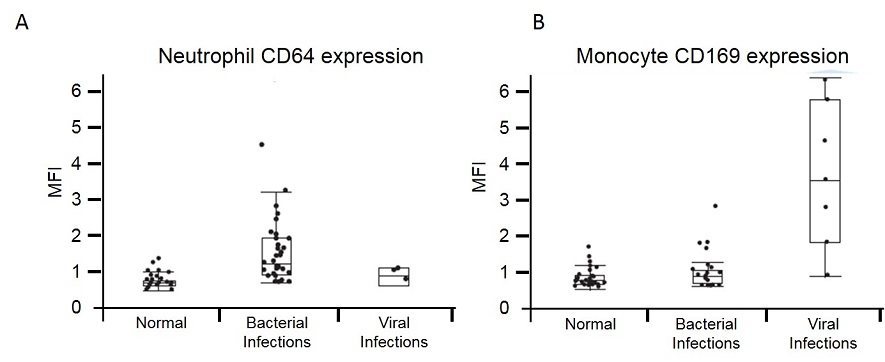
Livelli di CD64 dei neutrofili e CD169 dei monociti per tre gruppi. Espressione CD64 su neutrofili in condizioni normali (nessuna infezione), in infezioni batteriche e in infezioni virali, pannello A. Espressione CD169 su monociti in condizioni normali (nessuna infezione), in infezioni batteriche e in infezioni virali, pannello B. I dati sono presentati come media ed errori standard. I p-value sono calcolati tra gruppi usando il test t di Student e rivelano un aumento significativo dei biomarcatori se p ≤ 0.05.
Staining in Whole Blood
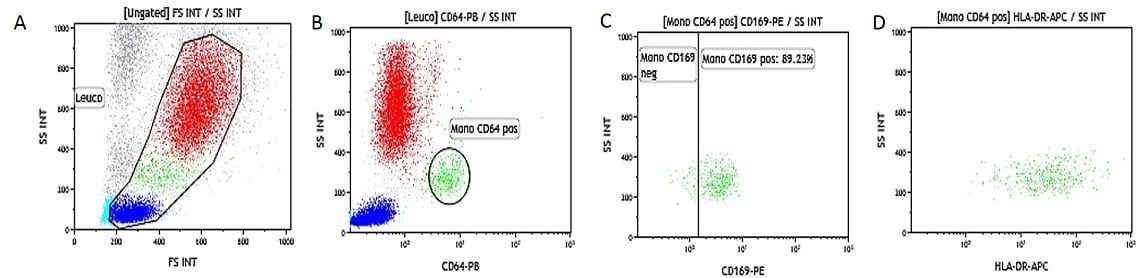
Sangue intero eparinizzato attivato con IFNβ. Dati ottenuti con 10 μL di sangue intero attivato IFNβ (16-20 ore di incubazione a 37 °C con IFNβ a 0,1 μg/mL concentrazione finale) e contemporaneamente marcato e lisato secondo la procedura descritta sopra. (A) SS/FS dot plot per gate leucociti, (B) SS/CD64-PB per gate monociti sui leucociti, (C) SS/CD169-PE dot plot gated sui monociti (gate è posto sul campione controllo non attivato), (D) SS/HLA-DR-APC dot plot gated sui monociti.
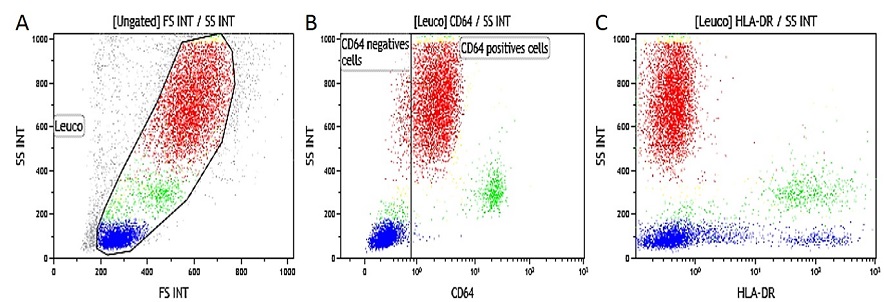
EDTA sangue intero IFNγ attivato. Dati ottenuti con 10 μL di sangue intero attivato con IFNγ (16-20 ore di incubazione a 37 ° C con IFNγ a 1 μg / mL concentrazione finale) e contemporaneamente marcato e lisato secondo la procedura descritta sopra. (A) SS/FS dot plot per i leucociti gate, (B) SS/CD64-PB gated sui leucociti (gate è posto sul campione di controllo non attivato), (C) SS/HLA-DR-APC dot plot gated sui leucociti.
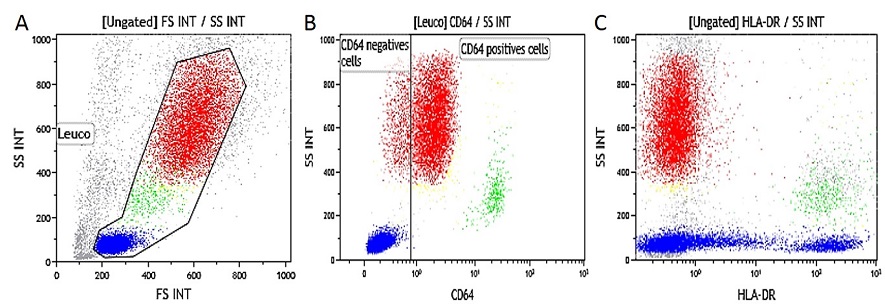
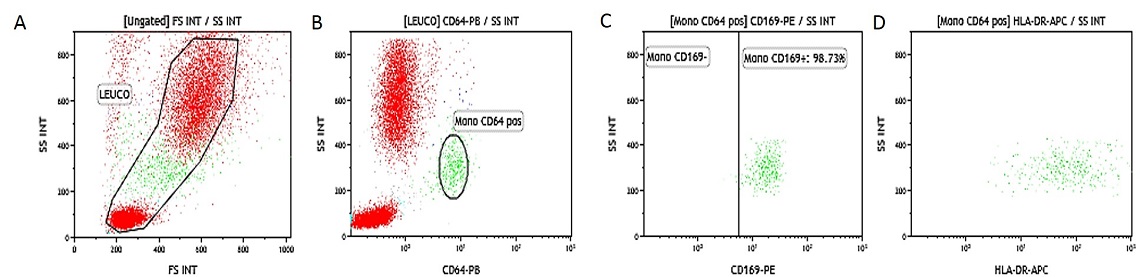
Sangue intero eparinizzato attivato con IFNγ . Dati ottenuti con 10 μL di sangue intero attivato IFNγ (16-20 ore di incubazione a 37 ° C con IFNγ a 1 μg / mL concentrazione finale) e contemporaneamente colorato e lisato secondo la procedura descritta sopra. (A) SS/FS dot plot per gate leucociti, (B) SS/CD64-PB gated su leucociti (gate è posto su campione di controllo non attivato, (C) SS/HLA-DR-APC dot plot gated su leucociti.
Referenze:
- Bourgoin P, Biéchelé G, Ait Belkacem I, Morange PE, Malergue F. Role of the interferons in CD64 and CD169 expressions in whole blood: Relevance in the balance between viral- or bacterial-oriented immune responses. Immun Inflamm Dis. 2020;8(1):106-123.
- Bourgoin P, Soliveres T, Ahriz D, et al. Clinical research assessment by flow cytometry of biomarkers for infectious stratification in an Emergency Department. Biomark Med. 2019;13(16):1373-1386.
- Shallcross LJ, Davies DS. Antibiotic overuse: a key driver of antimicrobial resistance. Br J Gen Pract. 2014 Dec;64(629):604-5.
- Ajmani S, Agarwal V, Gurjar M. State of Globe: Neutrophil CD64: Is It a Reliable Biomarker for Sepsis? J Glob Infect Dis. 2018 Apr-Jun;10(2):33-34.
- Akiyama H, Ramirez NP, Gibson G, et al. Interferon-Inducible CD169/Siglec1 Attenuates Anti-HIV-1 Effects of Alpha Interferon. J Virol. 2017;91(21):e00972-17.
- Stegelmeier AA, van Vloten JP, Mould RC, Klafuric EM, Minott JA, Wootton SK, Bridle BW, Karimi K. Myeloid Cells during Viral Infections and Inflammation. Viruses. 2019 Feb 19;11(2):168.
- Bedin AS et al. Monocyte CD169 expression as a biomarker in the early diagnosis of COVID-19, medRxiv 2020.06.28.20141556.
- Park MD. Macrophages: a Trojan horse in COVID-19? Nat Rev Immunol. 2020 Jun;20(6):351.
- Hadjadj J, Yatim N, Barnabei L, et al. Impaired type I interferon activity and inflammatory responses in severe COVID-19 patients. Science. 2020;369(6504):718-724.
- Rose T, Szelinski F, Lisney A, et al. SIGLEC1 is a biomarker of disease activity and indicates extraglandular manifestation in primary Sjögren's syndrome. RMD Open. 2016;2(2):e000292.
Esclusivamente per scopi di ricerca. Non è destinato ad essere utilizzato in procedure diagnostiche.

